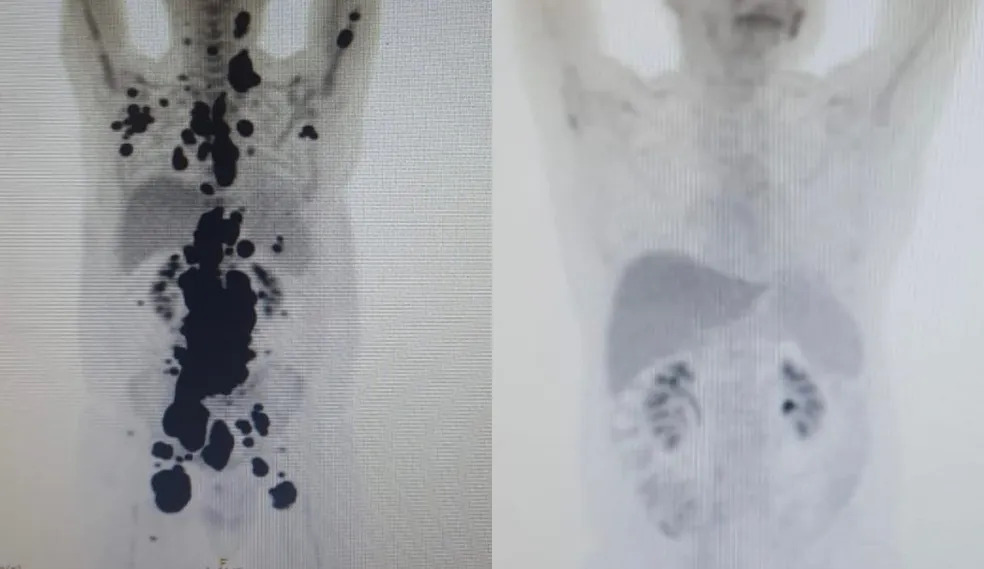
Objetivo da pesquisa com terapia celular avançada é avaliar a segurança no tratamento de pacientes com dois tipos de câncer: leucemia linfoide aguda B e linfoma não Hodgkin B.
O Ministério da Saúde liberou R$ 100 milhões para o financiamento da pesquisa de desenvolvimento da terapia celular CAR-T Cell, a técnica que combate o câncer no sangue com as próprias células de defesa do paciente modificadas em laboratório, na Fundação Hemocentro de Ribeirão Preto/USP em parceria com o Instituto Butantan, em São Paulo.
“Nosso objetivo é garantir à população mais carente o acesso aos tratamentos mais modernos contra o câncer”, afirmou ao g1 o secretário de Ciência, Tecnologia e Inovação e do Complexo Econômico-Industrial da Saúde, Carlos Gadelha. O apoio será por meio do Novo Programa de Aceleração ao Crescimento (PAC-Saúde).
Car-T Cell: entenda terapia celular contra câncer aplicada de forma experimental
O estudo clínico é financiado pelo Ministério da Saúde, com apoio de estrutura por parte do Butantan e investimento de pesquisa da Fapesp e do CNPq.
Segundo Rodrigo Calado, professor de medicina da USP e diretor-presidente do Hemocentro de Ribeirão Preto, no interior de São Paulo, a partir de janeiro e fevereiro do ano que vem, e por um período de 12 meses, os pacientes serão recrutados. Depois, acompanhados por mais 12 meses para uma análise dos resultados e a solicitação à Anvisa de registro do produto, que poderá ser disponibilizado ao SUS.
“Este tipo de projeto que coloca ideias científicas na prática, na vida das pessoas, só é possível porque é institucional e reúne grupos com expertises complementares: a USP, por meio da Faculdade de Medicina de Ribeirão Preto, o Hospital das Clínicas de Ribeirão Preto, por meio do seu Hemocentro, e o Instituto Butantan, com sua competência fabril farmacêutica”, diz Rodrigo.
“Também é fundamental reconhecer o apoio da Anvisa para o desenvolvimento e aprovação do estudo clínico, que pode conceder o registro a um produto nacional que pode mudar o tratamento de leucemias e linfomas no país”, completa o médico.
Em setembro, o g1 mostrou que o Hemocentro de Ribeirão Preto/USP foi escolhido pela Agência Nacional de Vigilância Sanitária (Anvisa) para ser o responsável pelo projeto-piloto no desenvolvimento de produtos de terapia avançada.
O estudo clínico de fase 1/2 vai incluir 81 pacientes com leucemia linfoide aguda de células B e linfoma não Hodgkin de células B, de forma gratuita (entenda mais abaixo).
Pacientes tratados
Já foram tratados com essa terapia de células CAR-T desenvolvidas na USP e no Hemocentro de Ribeirão Preto 20 pacientes com leucemia ou linfoma, sendo que 14 deles continuam bem, de acordo com os médicos. Todos eram casos graves para os quais não havia mais opção terapêutica.
Vamberto Luiz de Castro, o primeiro paciente a realizar o tratamento em 2019, teve remissão total, mas morreu pouco tempo depois em um acidente doméstico.
Outro caso que repercutiu neste ano foi o de Paulo Peregrino, de Niterói, no Rio de Janeiro, que fez o tratamento de forma compassiva, ou seja, por meio de uma autorização da Anvisa, de forma individualizada, para pessoas que já tinham esgotado todos os tratamentos aprovados possíveis.
O publicitário combatia o câncer havia 13 anos e teve remissão completa do linfoma em 30 dias com CAR-T Cell. Paulo estava prestes a receber cuidados paliativos quando, entre março e abril, foi o 14º paciente a ser tratado pela terapia, em São Paulo.
Quem pode se candidatar?
A parceria entre as instituições resultou na construção de duas unidades do Núcleo de Terapia Avançada (Nutera) em Ribeirão Preto e na capital paulista. Apenas a “fábrica de células” de Ribeirão Preto está em operação e será responsável por atender a demanda de participantes do estudo. No futuro, poderão ser atendidos até 300 pacientes ao ano.
O estudo clínico é focado especificamente em pacientes com leucemia linfoide aguda de células B e linfoma não Hodgkin de células B que não responderam ou apresentaram o retorno da doença após a primeira linha de tratamento convencional, como quimioterapia e o transplante de medula óssea.
A técnica brasileira não tem efetividade em outros tipos de cânceres sólidos, além dos tipos citados acima.
Segundo os pesquisadores, o paciente que acredita preencher os requisitos deve conversar com o seu médico e pedir que ele entre em contato pelo e-mail: terapia@hemocentro.fmrp.usp.br.
Deve ser anexado o relatório de saúde do candidato, e o material será avaliado pelas equipes. Se o caso se enquadrar no estudo, o médico responsável pelo paciente será avisado.
Fonte: G1